이 세계의 많은 원자들은 이온 상태로 전하를 띄어 다른 원자들과 상호작용한다. 그렇기 때문에 많은 과학에서 이온에 대한 이해는 필수적이라 할 수 있다. 이 글에서는 그러한 이온과 이온 반응에 대해 다룰 것이다.
이온
원자는 양성자, 중성자로 이루어진 핵과 전자로 이루어져 있다.
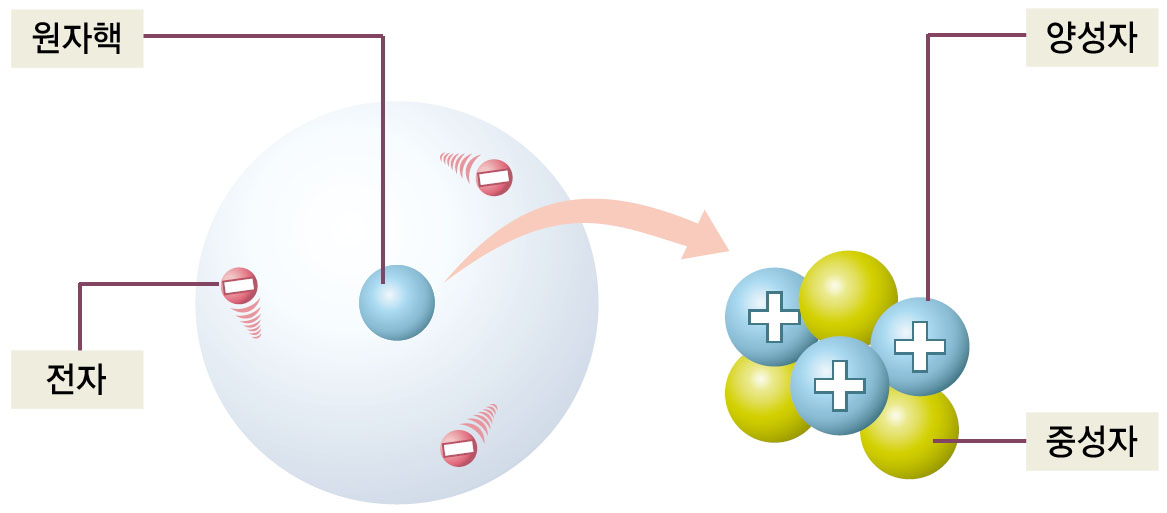
일반적으로 원자 안에는 +전하를 띄는 양성자와 -전하를 띄는 전자의 개수가 같아서 전기적으로 중성을 띤다.
하지만, 원자들은 옥텟 규칙(최외곽 전자 수가 꽉 차있는 원자가 가장 안정하다.)을 만족하려 하기 때문에 전자를 더 얻거나, 빼앗기는 방향으로 최외곽 전자를 꽉 채우려고 한다. 그렇게 양성자와 전자의 개수가 달라지고 원자는 전하를 띄게 된다. 이러한 방식으로 전기를 띄는 원자를 이온이라고 하며 원자에 윗 첨자로 이온이 되면서 변화된 전자 개수를 적어준다.
전자는 음극이기때문에 전자를 얻은 원자는 음극을 띄고 전자를 얻은 이온을 음이온이라고 한다. 같은 원리로 전자를 빼앗겨 생긴 이온은 양극을 띄고 양이온이라고 한다.
예를 들어, 전자를 2개 받아 생긴 산소 음이온은 $\rm O^{2-}$라고 쓰며 전자를 1개 내보내 생긴 칼륨 양이온은 $\rm K^+$이라고 쓴다.
참고로, 전자의 이동으로 전하를 띄는 원자와 분자를 모두 이온이라 한다.
여러가지 이온들과 분자이온
다음은 여러가지 이온들이다. 잘 기억해 두고, 필요할 때 쓸 수 있도록 하자.
| 이온식 | 이온이름 | 이온식 | 이온이름 | 이온식 | 이온이름 | 이온식 | 이온이름 |
| $\rm Ag^+$ | 은이온 | $\rm Cu^{2+}$ | 구리이온 | $\rm I^-$ | 아이오딘화이온 | $\rm CH_3COO^{-}$ | 아세트산이온 |
| $\rm H^+$ | 수소이온 | $\rm Pb^{2+}$ | 납이온 | $\rm Cl^-$ | 염화이온 | $\rm MnO_4^{-}$ | 과망가니즈산이온 |
| $\rm K^+$ | 칼륨이온 | $\rm Zn^{2+}$ | 아연이온 | $\rm OH^-$ | 수산화이온 | $\rm CrO_4^{2-}$ | 크로뮴산이온 |
| $\rm Na^+$ | 나트륨이온 | $\rm Cr^{2+}$ | 크로뮴이온 | $\rm O^{2-}$ | 산화이온 | $\rm BO_3^{3-}$ | 붕산이온 |
| $\rm NH_4^+$ | 암모니아이온 | $\rm Cd^{2+}$ | 카드뮴이온 | $\rm S^{2-}$ | 황화이온 | $\rm PO_4^{3-}$ | 인산이온 |
| $\rm Ba^{2+}$ | 바륨이온 | $\rm Mg^{2+}$ | 마그네슘이온 | $\rm NO_3^{-}$ | 질산이온 | ||
| $\rm Ca^{2+}$ | 칼슘이온 | $\rm Al^{3+}$ | 알루미늄이온 | $\rm CO_3^{2-}$ | 탄산이온 | ||
| $\rm Fe^{2+}$ | 철이온 | $\rm SO_4^{2-}$ | 황산이온 |
앙금의 생성
일반적으로 이온결합물은 수용액속에서 이온상태로 존재하게 된다. 하지만 일부는 물에 녹지 않고 침전물의 형태로 존재하는데 이를 앙금이라고 한다. 앙금의 종류는 다음과 같다.
| 색깔 | 종류 | ||
| 흰색 | $\rm AgCl, Ag_2CO_3, Ag_2SO_4$ | $\rm BaSO_4, BaCO_3$ | $\rm CaSO_4, CaCO_3$ |
| 노란색 | $\rm AgI, PbI_2, CdS$ | ||
| 검정색 | $\rm FeS, CaS, PbS$ | ||
앙금의 색과 화학식또한 잘 기억해 두었다가 필요할때 활용할 수 있도록 하자.
이온반응식
이온결합물들은 서로 반응하여 다른 이온이나 앙금을 만들기도 한다.
알짜이온이란 반응에 실제로 참여하는 이온으로써 앙금을 생성하는데 쓰인 이온들을 말한다.
구경꾼이온이란 반응에 참여하지 않았고 결과적으로 앙금을 만들지 않은 이온들을 말한다.
다음 예를 보자.
| $\rm {AgNO_3}_{(aq)} + {NaCl}_{(aq)} \rightarrow AgCl + {NaNO_3}_{(aq)}$ |
위 반응식에서는 질산은과 염화나트륨이 반응하여 염화은 앙금과 질산나트륨을 만드는 모습이다.
앙금의 생성에 관여한 이온은 $\rm Ag^+, Cl^-$이고 그렇지 않은 이온들은 $\rm Na^+, NO_3^-$이다. 따라서 알짜이온은 $\rm Ag^+, Cl^-$가 되고 구경꾼 이온은 $\rm Na^+, NO_3^-$가 되는 것이다.
반응식의 여러 이온중에서 알짜이온만 표기한 반응식을 알짜이온반응식이라고 한다. 위 반응식의 알짜이온반응식을 다음과 같다.
| $\rm Ag^+ + Cl^- \rightarrow AgCl$ |
이 글에서는 이온의 정의와 앙금, 그리고 앙금을 만드는 이온반응식에 대해 알아보았다. 실제로 이온들이 모여 만들어내는 현상은 산화환원, 산과 염기등 다양하다. 그러니, 이 글에서 배운 내용을 잘 알아두어 연습해두자.
